이온결합, 공유결합, 금속결합

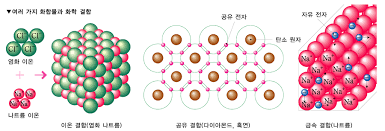
이온결합 이란 음이온이 정전기적 인력으로 결합해서 생기는 화학결합으로 대응되는 화학결합은 공유결합
이온결합 예로 소금같이 양성이 강한 금속과 음성이 강한 비금속 결합물
공유결합은 주기율표 직선 지향요소에서 관찰되며 원자 사이 전자 교환을 포함
금속결합은 금속 및 로이드 광물과 합금 사이에 발생하는 일종의 화학적 결합
● 이온결합
이온결합은 강한 정전기 힘과 양이온과 음이온 사이의 연결로 정의. 하나 이상의 전자를 얻거나 잃는 원자는 이온
전자를 잃는 원자는 양전하 양이온이라고 불리며 전자를 얻는 원자는 음전하 음이온. 이러한 유형의 결합에서 양이온은 음이온에 끌리는 반면 음이온은 음이온에 끌린다.
우리는 반대 이온이 옷을 입고 이온이 거부한다고 말할 수 있다. 서로에 대항하여 이온은 이온 사이의 정적 경이로움의 존재로 인해 이온 결합을 생성. 금속은 전자가 거의 없으며, 그 다음 전자를 잃어 버리고, 금속은 희토류 가스 구성에 도달하여 뼈 규칙을 준수. 반면에 비금속 원자가 껍질은 8개의 전자만 가지고 있으며, 전자를 받아 들인 다음 희토류 가스 구성을 얻는다.
이온 결합의 총 전하는 0이어야 한다. 옥 규칙을 준수하기 위해 전자 수용 또는 기여는 1보다 클 수 있다. 염화나트륨(NaCl)의 일반적인 예는 말초 나트륨 궤도의 전자와 초탐색기의 7개의 전자를 갖는 염소를 갖는 것이다.
따라서 염소는 뼈를 완성하기 위해 단 하나의 전자만 필요로 한다. 두 원자(Na와 Cl)가 염소에 전자에 접근하면 나트륨이 서로 주어진다. 그런 다음 나트륨 전자가 손실되면 양의 하중이 되고 전자 염소를 받아들이면 음의 하중이 되어 염화물 이온이 된다.
● 공유결합
비 결합 금속 인의 주기율표의 직선 지향 요소에서 공유 결합이 관찰된다. 공유 결합은 원자 사이의 전자 교환을 포함한다. 공유 전자 쌍은 분자라고 불리는 두 원자의 핵 주위에 새로운 궤도를 만든다.
원자의 두 핵 사이의 강한 에너지를 차단하는 기적적인 힘이 있으며, 결합 과정에서 총 에너지가 개별 원자 근처의 전하 값보다 작을 때 결합이 형성.
공유 결합은 분자 결합이라고도 한다. 질소 (N2), 수소 (H2), 물 (H2O), 암모니아 (NH3), 염소 (Cl2) 및 불소 (F2)는 공유 결합 화합물의 몇 가지 예이다. 전자 공유는 원자가 안정한 외부 전자 스케일 구성을 얻을 수 있게 한다.
예를 들어, 물은 H2O와 같은 화학식을 가지고 있으며, 각 수소와 산소 분자 사이에 공유 결합을 발견하고 수소와 산소 사이에 두 개의 전자를 공유.
수소 분자로서 H2는 산소에 공유 결합으로 결합된 두 개의 수소 원자를 함유하고 있다. 이것은 전자의 외부 궤도에 발생하는 원자 사이의 인간 자원.
● 금속결합
금속, 로이드 광물, 합금 사이에 발생하는 일종의 화학적 결합. 전자가 양이온 구조를 공유하는 양전하 원자 사이의 연결은 열과 전기에 좋은 전도체로 간주.
이 범주에서 전자는 각 금속 원자의 외부 지각이 이웃 원자를 방해하기 때문에 금속 원자가 여전히 전체 공간에서 다른 공간으로 자유롭게 움직이고 있다고 말할 수 있다.
원자는 비공식적인 전자 상품이거나 자유 전자의 존재이기 때문에 Paul Drod는 1900년에 "전자 바다"라는 이름을 발표했다. 금속의 다양한 특성은 융합 및 높은 비등점, 관성, 관성 및 우수한 전도성 내구성, 강하고 낮은 금속 결합 및 낮은 변동.

잡스9급 PDF 교재

✽ 책 구매 없이 PDF 제공 가능
✽ adipoman@gmail.com 문의
- 공무원 국어 PDF 다운로드
- 공무원 영어 PDF 다운로드
- 공무원 한국사 PDF 다운로드
- 공무원 행정학 PDF 다운로드
- 공무원 행정법 PDF 다운로드
- 헌법, 형법, 형소법, 경찰학, 민법, 상법 PDF 다운로드
- 소방학개론, 소방관계법규 PDF 다운로드
- 경영학, 경제학, 회계학 PDF 다운로드
- 교육학개론 PDF 다운로드